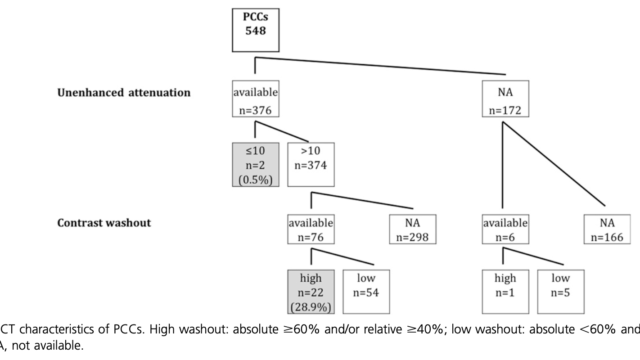
・褐色細胞腫の約70%が副腎偶発腫瘍としてみつかる。
・副腎偶発腫瘍としてみつかる褐色細胞腫は、症候例と比較して、高齢(62歳vs42歳)・小さい腫瘍径(42mm vs 60mm)・メタネフリン低値(正常上限の5倍 vs 15倍)・遺伝子変異率低値(15.3% vs 42.9%)である。
・2cm以下の副腎偶発腫瘍でみつかる褐色細胞腫ではメタネフリンは正常上限の2倍以下でも否定できない。CT値が10HU以上の場合は注意。
・MIBGシンチ陰性例は全体の6%。
イギリスのQueen Elizabeth Hospital Birminghamで2010年から2022年の間に診療された褐色細胞腫の患者の診療録を後ろ向きに評価。褐色細胞腫の診断は病理もしくは血中または尿中メタネフリンの上昇とCT・MRIでの副腎腫瘍、MIBGシンチ陽性でなされた。
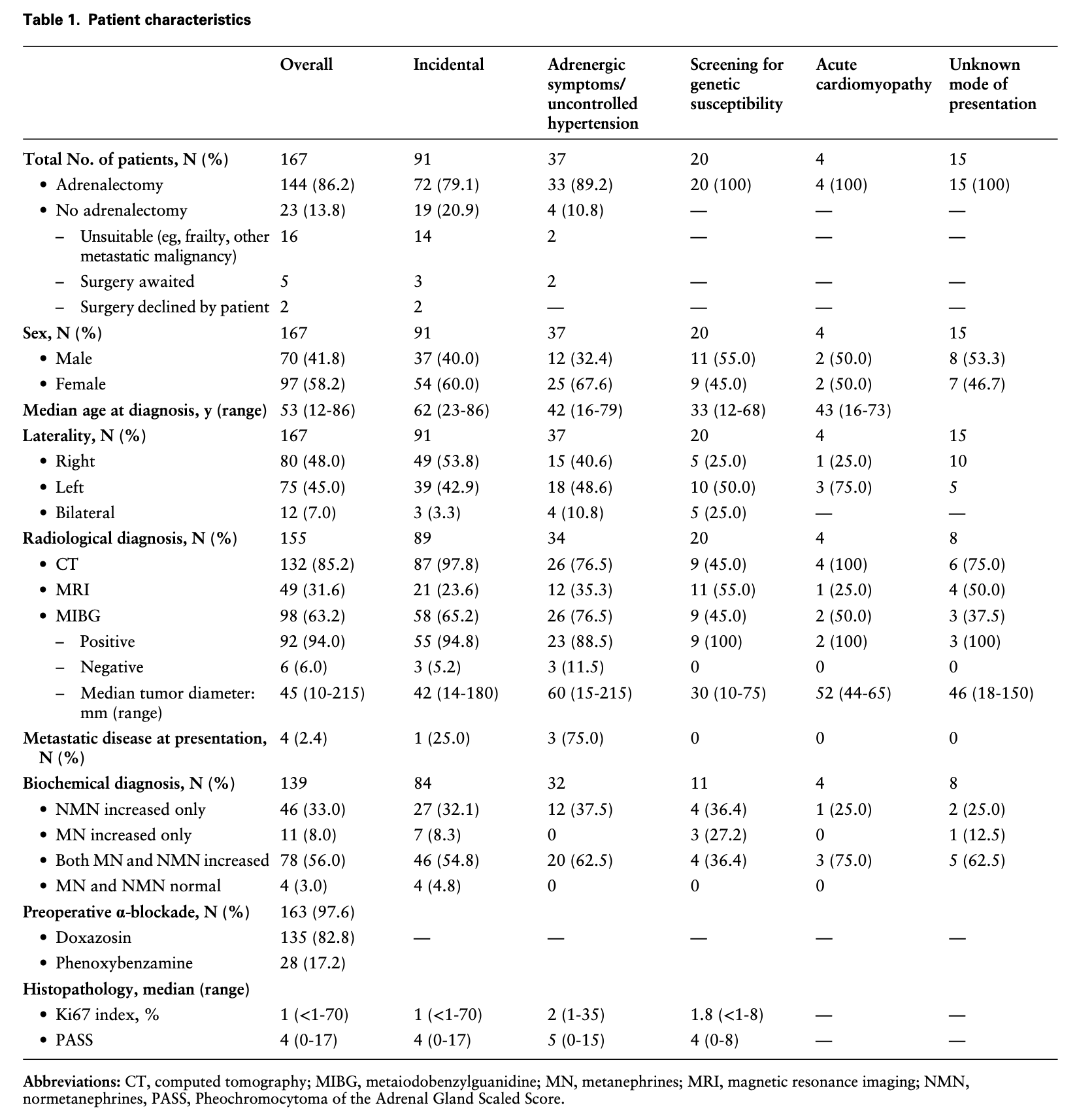
167名の褐色細胞腫のうち女性が58.2%、診断時の年齢の中央値は53歳(12-86歳)。
副腎切除術は144名(86.2%)の患者で実施され、全例病理で証明された。
残りの23名(13.8%)は手術待ちの患者5名、フレイルやStageⅣの悪性腫瘍の合併などで手術ができない患者16名、手術辞退が2名であった。褐色細胞腫は右側が80例(48.0%)、左側75例(45.0%)、両側性が12例(7.0%)であった。診断時に遠隔転移を認めたのは4例(2.4%)のみだった。
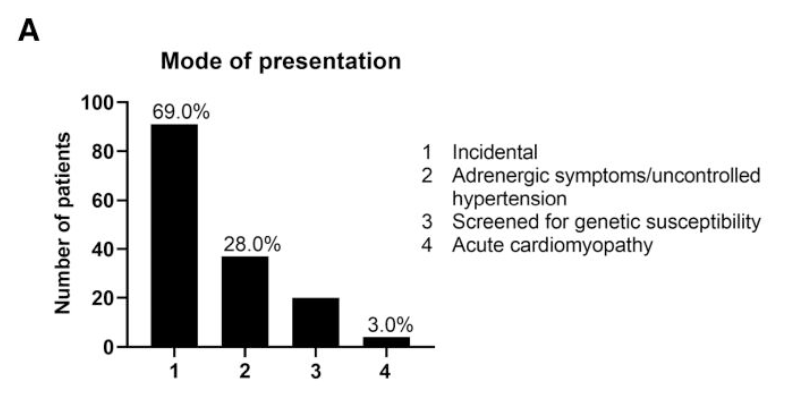
152名の診断の契機のうち、20名(13.2%)が遺伝的スクリーニングであり、副腎偶発腫瘍の精査で診断された褐色細胞腫が91名(69.0%)と最多であった。次いで症候性/治療抵抗性高血圧が37名(28.0%)、急性心筋症が4名(3.0%)であった。
→副腎偶発腫瘍が約7割、症候性/治療抵抗性高血圧が約3割。
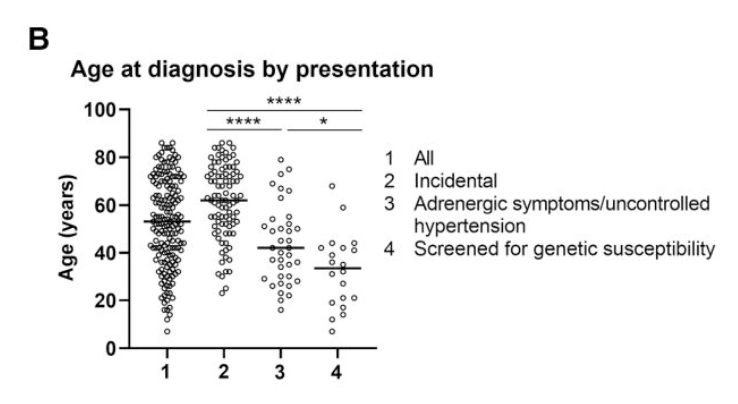
診断時の年齢の中央値と範囲(副腎偶発腫瘍>症候性>遺伝スクリーニング)
副腎偶発腫瘍として発見された褐色細胞腫:62歳(23-86歳)
症候性/治療抵抗性高血圧を呈した褐色細胞腫:42歳(16-79歳)
遺伝的スクリーニングで発見された褐色細胞腫:33歳(12-68歳)
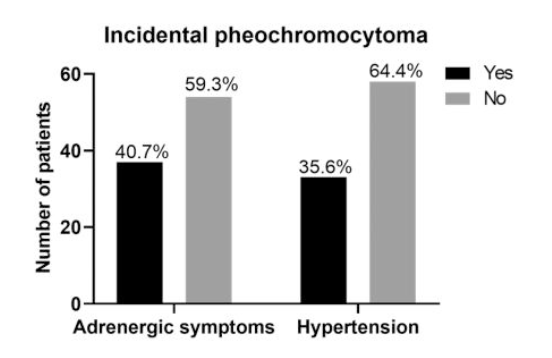
症状
副腎偶発腫瘍として見つかった褐色細胞腫の患者の40.7%に典型的な交感神経症状を認めた。これらの患者を除くとピュアな副腎偶発腫瘍であった褐色細胞腫は54例(32.3%)であった。
→褐色細胞腫の症状が非特異的であり見逃されている可能性がある。
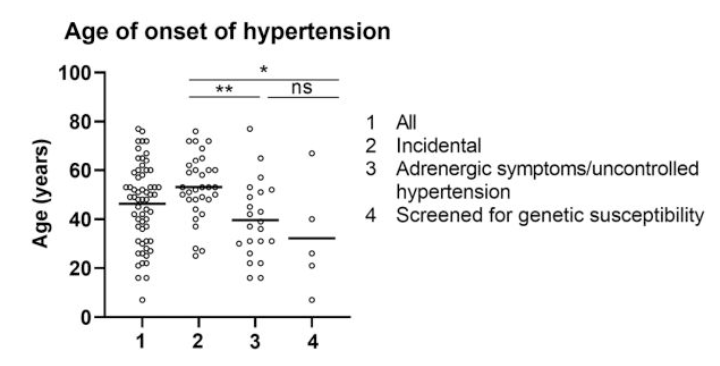
高血圧の診断年齢の中央値
副腎偶発腫瘍として発見された褐色細胞腫:53歳(22-72歳)
症候性/治療抵抗性高血圧を呈した褐色細胞腫:38歳(16-77歳)
診断時の年齢は副腎偶発腫瘍群のほうが高かったが、収縮期血圧・拡張期血圧・平均動脈圧は二群間に差はなかった。
→症候性の方が高血圧の発症が早い。
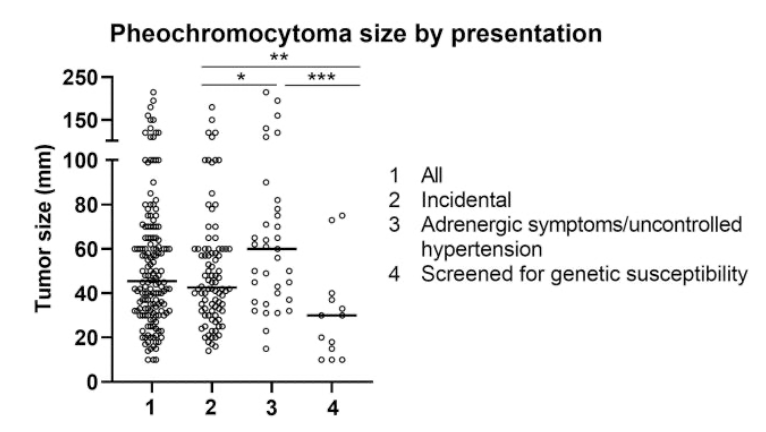
全体の中央値は45mm(10-215mm)
副腎偶発腫瘍:42mm(14-180mm)
症候性/治療抵抗性高血圧:60mm(15-215mm)
遺伝スクリーニング:30mm(10-75mm)
腫瘍径は症候性/治療抵抗性高血圧>副腎偶発腫瘍>遺伝スクリーニングの順で大きかった。
CT値
CTで発見された131例のCT値の中央値は33HU(10-77HU)。
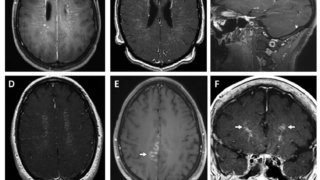
MRI T2高信号
MRIを撮影された43例のうち、22例(52.4%)に認めた。
MIBGシンチグラフィ
98例(65.7%)に術前にMIBGシンチが実施され、92例(94%)に集積を認めたが、6例(6%)はメタネフリン高値かつ病理で確定診断されたがMIBIシンチ陰性であった。
→CT値はやはり10HU以上、MRIのT2高信号は半分程度、MIBGシンチは6%偽陰性。
134例(80.2%)は血中メタネフリン高値で診断され、尿中メタネフリン値のみで診断されたのは33例(19.8%)のみだった。両方測定されたのは21例のみで、強く相関していた。
ノルメタネフリン優位が75/139(54.0%)、メタネフリン優位が60/139(43.2%)。
ノルメタネフリンのみ高値46例(33.0%)、メタネフリンのみ高値11例(8.0%)、両方とも高値78例(56.0%)、両方とも正常が4例(3.0%)。ドパミン代謝産物である3-メトキシチラミン優位高値の患者はいなかった。
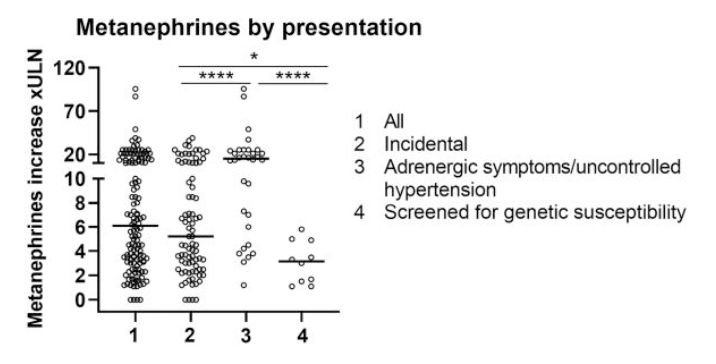
メタネフリン上昇の中央値は5倍(1-96倍)。
症候性/治療抵抗性高血圧>副腎偶発腫瘍>遺伝スクリーニング。
副腎偶発腫瘍:5倍
症候性/治療抵抗性高血圧:15倍
遺伝スクリーニング:3倍
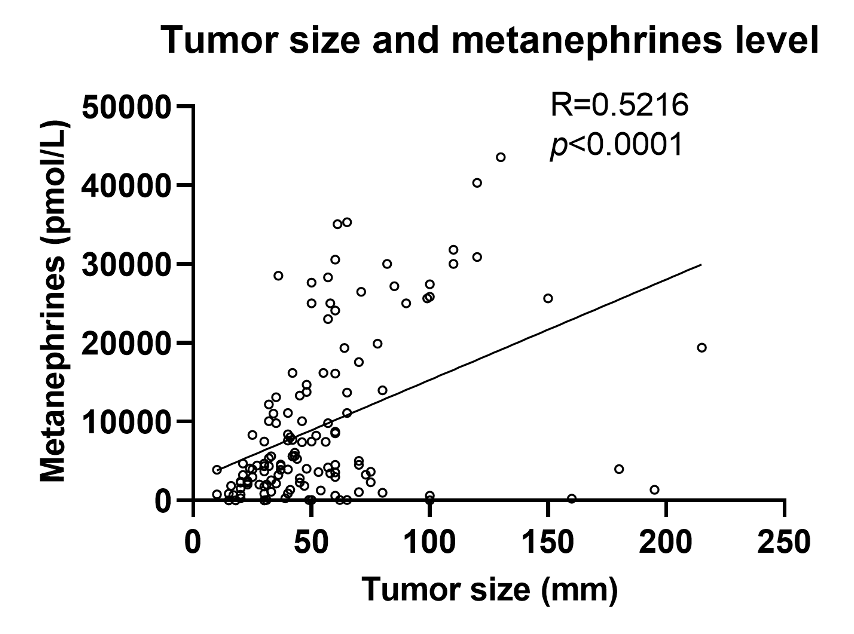
腫瘍径とメタネフリン値の間に相関あり(R=0.52, P< .0001)
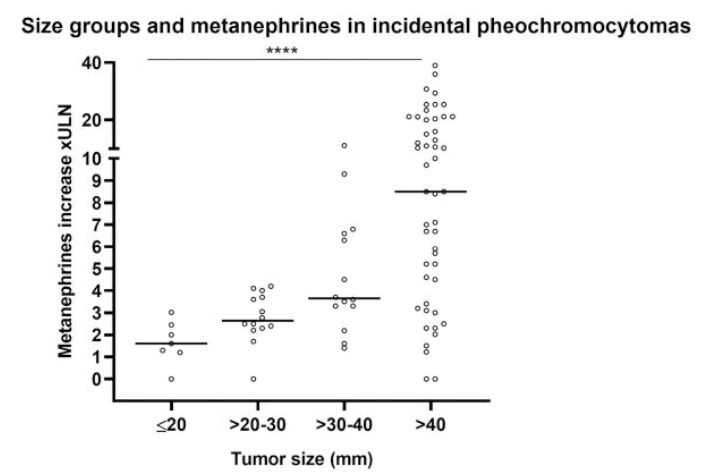
副腎偶発腫瘍群でも同様で、メタネフリン高値の中央値は20mm以下では2ULN以下、20-30mmでは2-3ULN、30-40mmでは3-4ULN、40mm以上では8-9ULNと比例した。
→2cm以下の副腎偶発腫瘍としてみつかる褐色細胞腫の場合、メタネフリンは正常上限の2倍以下でも否定できない。
術前マネジメント
褐色細胞腫の診断がつきしだいαブロッカーによる治療が行われた(163例, 97.6%)。ドキサゾシン82.8%、フェノキシベンザミン17.2%。
手術を行った患者のうち4例(2.4%)は術前にα遮断薬による治療を行わなかった。2例はメタネフリンが正常、1例は低血圧、1例は腎癌の診断で手術され術後に褐色細胞腫と診断された。
α遮断薬は血圧120/80mmHg以下を目標に、症状に応じて調整された。
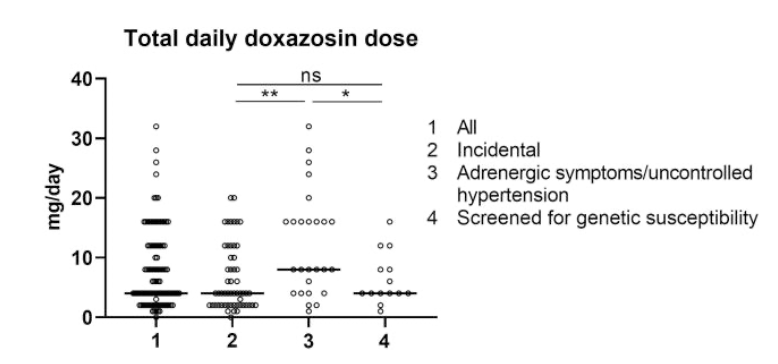
ドキサゾシンの術前の投与量は6mg(1-32mg)、フェノキシベンザミンは40mg(10-90mg)だった。副腎偶発腫瘍・遺伝スクリーニング群は4mg(1-20mg)、症候性/治療抵抗性高血圧群は8mg(1-32mg)と量に違いがあった。ドキサゾシン量と腫瘍径の間に相関はなかった。
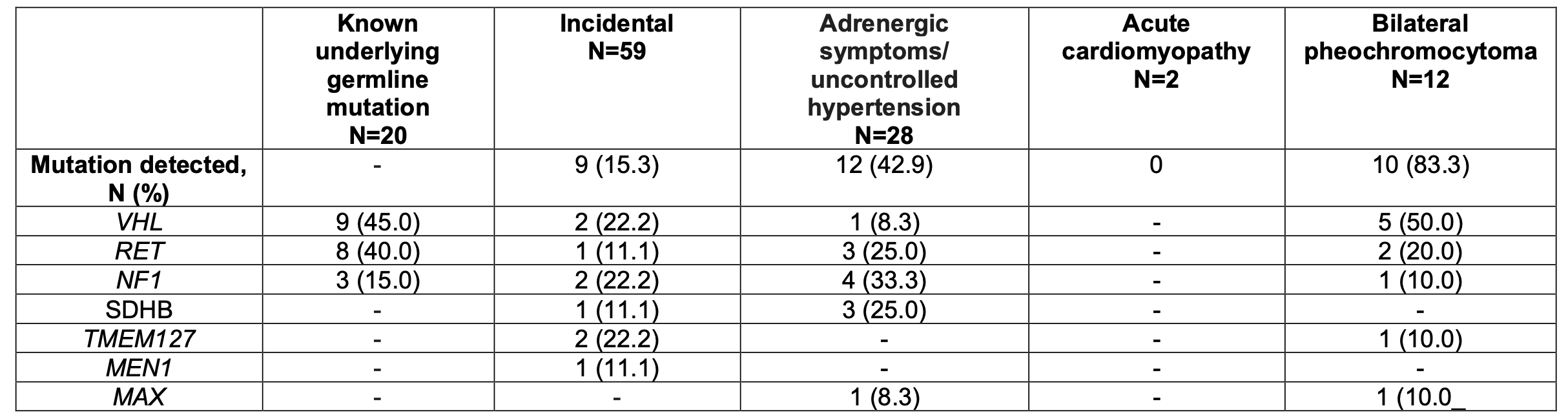
遺伝的背景がない147例のうち、103例(70%)に遺伝子検査が行われ、21例(20.4%)に遺伝子変異を認めた。変異はNF1(6例、28.6%)、RET(4例、19.0%)、SDHB(4例、19.0%)、VHL(3例、14.3%)、TMEM127(2例、9.5%)、MEN1(1例、4.8%)、MAX(1例、4.8%)であった。
91例の副腎偶発腫瘍として発見された褐色細胞腫のうち、59例(64.8%)が遺伝子検査を受け、9例(15.3%)に変異を認めた。
一方、症候性/治療抵抗性高血圧を呈した褐色細胞腫のうち、28/37(75.7%)が遺伝子検査を受け、12例(42.9%)に変異を認めた。
両側褐色細胞腫12例のうち、10例(83.3%)に既知の遺伝子変異があり、1例に術後の遺伝子検査で変異が認められた。
遺伝スクリーニング群の20例の内訳は、VHL9例(45%)、RET8例(40%)、NF1 3例(15%)だった。
→偶発腫瘍群の方が遺伝子変異の割合は少ない。両側性は遺伝子変異の可能性が高い。
127例(76%)の病理データがあり、Ki67-indexの中央値は1%(<1%-70%)で症候性/治療抵抗性高血圧群(2%, 範囲1-35%)のほうが、副腎偶発腫瘍群(1%, 範囲<1%-70%)より高かった。
PASSの中央値は4で、各群で違いはなかった。
フォローアップ期間は36ヶ月(1-179ヶ月)。
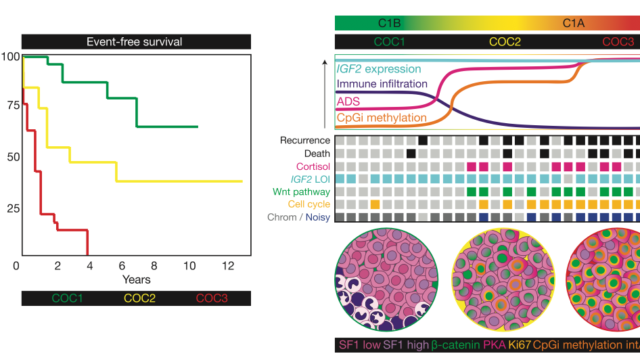
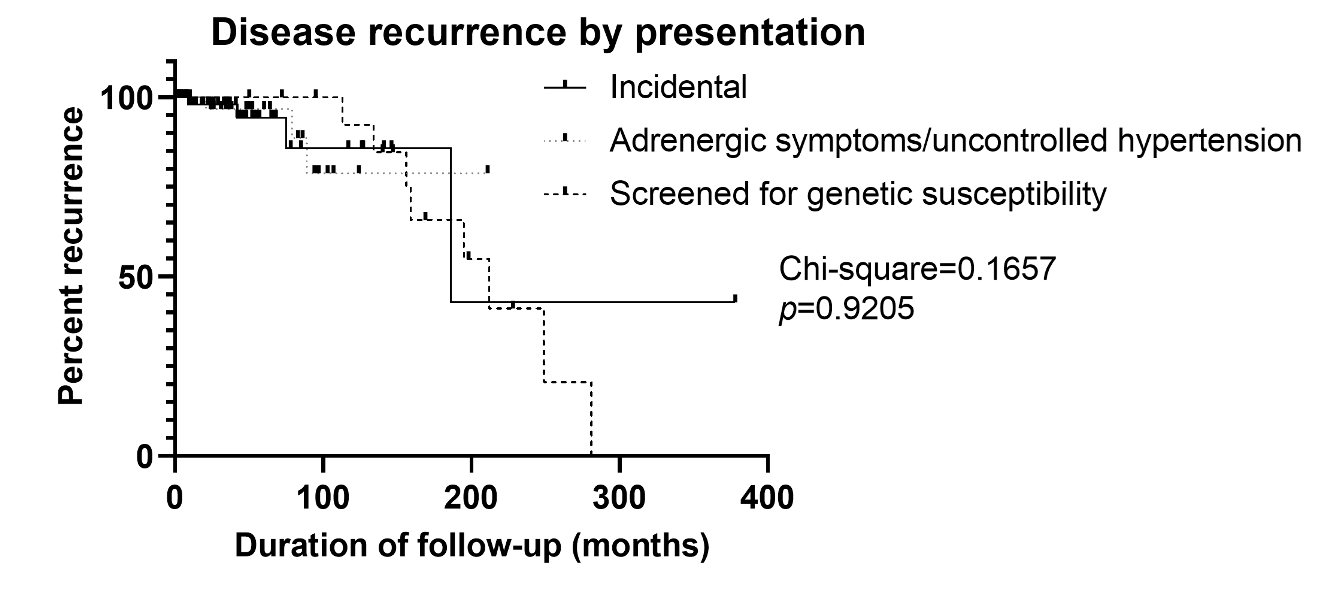
遠隔転移病変は17例(10.2%)に認められ、副腎偶発腫瘍群4例(4.4%、フォローアップ期間23ヶ月、範囲1-146ヶ月)、症候性/治療抵抗性高血圧群3例(8.1%、フォローアップ期間36ヶ月、範囲1-179ヶ月)、遺伝スクリーニング群8例(40%、フォローアップ期間113ヶ月、範囲2-169ヶ月)であり、再発において各群に違いはなかった。再発までの中央期間は80ヶ月(6-153ヶ月)であった。
→再発に違いはない。再発までの中央期間は約6-7年。
・褐色細胞腫の約70%が副腎偶発腫瘍としてみつかる。
・副腎偶発腫瘍としてみつかる褐色細胞腫は、症候例と比較して、高齢(62歳vs42歳)・小さい腫瘍径(42mm vs 60mm)・メタネフリン低値(正常上限の5倍 vs 15倍)・遺伝子変異率低値(15.3% vs 42.9%)である。
・2cm以下の副腎偶発腫瘍でみつかる褐色細胞腫ではメタネフリンは正常上限の2倍以下でも否定できない。CT値が10HU以上の場合は注意。
・MIBGシンチ陰性例は全体の6%。